เทคโนโลยีการระบุหมายเลขเฉพาะประจำอุปกรณ์ทำให้การอ่านหมายเลขประจำทางการแพทย์และบาร์โค้ดเป็นไปโดยอัตโนมัติ
Contributed By DigiKey's North American Editors
2023-10-26
ในปี 2013 สำนักงานคณะกรรมการอาหารและยาแห่งสหรัฐอเมริกา (FDA) ได้นำระบบการระบุหมายเลขเฉพาะประจำอุปกรณ์หรือกฎ UDI มาใช้ กฎนี้มีจุดมุ่งหมายเพื่อปรับปรุงความปลอดภัยของผู้ป่วยโดยจัดให้มีวิธีการติดตามและระบุอุปกรณ์ทางการแพทย์ที่สอดคล้องกัน โดยใช้เอกสารที่ทันสมัย ณ จุดการผลิต จัดจำหน่าย และใช้งาน เช่นเดียวกับข้อกำหนดกฎระเบียบด้านอุปกรณ์การแพทย์ในยุโรปหรือกฎระเบียบที่คล้ายกันในประเทศอื่นๆ โดยที่กฎ UDI ของสหรัฐอเมริกาช่วยเพิ่มความแม่นยำในการรายงานและอำนวยความสะดวกในการวิเคราะห์ในกรณีที่มีการเรียกคืนหรือเหตุการณ์ไม่พึงประสงค์
ตั้งแต่วันที่ 24 กันยายน 2023 เป็นต้นไป FDA จะบังคับใช้รหัสรายการที่เกี่ยวข้องกับสุขภาพแห่งชาติและหมายเลขรหัสยาในฉลากอุปกรณ์และแพ็คเกจ ผลิตภัณฑ์ทางการแพทย์ใดๆ ที่มีฉลากนับจากวันนั้นหรือหลังจากนั้นจะต้องปฏิบัติตามข้อบังคับของ UDI โดยสมบูรณ์ การบังคับใช้นี้จะส่งผลกระทบต่อผลิตภัณฑ์ต่อไปนี้:
- ผลิตภัณฑ์ที่มีความสำคัญต่อชีวิตประเภท 3 เช่น เครื่องกระตุ้นหัวใจและขาเทียมแบบฝัง
- ผลิตภัณฑ์ที่มีความสำคัญปานกลางประเภท 2 เช่น หลอดฉีดยา สายสวน และไหมเย็บดูดซับได้
- ผลิตภัณฑ์ที่มีความเสี่ยงต่ำประเภทที่ 1 เช่น ไหมขัดฟัน เสื้อกาวน์ทางการแพทย์ และหน้ากากออกซิเจน
การบังคับใช้ข้อบังคับโดยสมบูรณ์หมายความว่าหากอุปกรณ์ทางการแพทย์ไม่มีบาร์โค้ดที่สแกนได้ จะไม่ถือว่าเป็นผลิตภัณฑ์ที่ถูกต้อง/ไม่สามารถใช้งานได้อีกต่อไป แม้ว่าจะมีฉลากที่มนุษย์สามารถอ่านได้ และแม้ว่าโดยทั่วไปถือว่าผลิตภัณฑ์นั้นเป็น ผลิตภัณฑ์ผู้ใช้ส่วนใหญ่ระบุได้ง่าย การบังคับใช้เต็มรูปแบบนี้จะกระตุ้นให้อุตสาหกรรมการแพทย์และการเรียกเก็บเงินค่าประกันสุขภาพนำไปใช้อย่างครอบคลุม
 รูปที่ 1: เครื่องตรวจสอบบาร์โค้ด Direct Part Mark (DPM) แบบพกพาบางรุ่นมีระบบแสงขั้นสูงและซอฟต์แวร์อื่นๆ เพื่อค้นหาบาร์โค้ดโดยอัตโนมัติและวนผ่านการตั้งค่าเพื่อปรับการอ่านเครื่องหมาย DPM เฉพาะและวัสดุที่ถือไว้ที่มีอยู่ให้เหมาะสมที่สุด ในความเป็นจริงแล้ว LVS-9585 ที่แสดงไว้ในที่นี่สามารถตรวจสอบทั้งส่วน DPM และฉลากที่พิมพ์ออกมาเพื่อการวิเคราะห์และการรายงานที่ครอบคลุม (แหล่งที่มาภาพ: Omron Automation)
รูปที่ 1: เครื่องตรวจสอบบาร์โค้ด Direct Part Mark (DPM) แบบพกพาบางรุ่นมีระบบแสงขั้นสูงและซอฟต์แวร์อื่นๆ เพื่อค้นหาบาร์โค้ดโดยอัตโนมัติและวนผ่านการตั้งค่าเพื่อปรับการอ่านเครื่องหมาย DPM เฉพาะและวัสดุที่ถือไว้ที่มีอยู่ให้เหมาะสมที่สุด ในความเป็นจริงแล้ว LVS-9585 ที่แสดงไว้ในที่นี่สามารถตรวจสอบทั้งส่วน DPM และฉลากที่พิมพ์ออกมาเพื่อการวิเคราะห์และการรายงานที่ครอบคลุม (แหล่งที่มาภาพ: Omron Automation)
หน่วยงานที่ทำสัญญา (ผู้ถือตราสินค้า) เป็นผู้รับผิดชอบ
ในสหรัฐอเมริกา เจ้าของทรัพย์สินทางปัญญาและตราสินค้าที่ติดต่อกับผู้ใช้ผลิตภัณฑ์ทางการแพทย์ทุกชิ้นจะต้องรับผิดชอบต่อความถูกต้องและคุณภาพของรหัส UDI สิ่งนี้มีความสำคัญอย่างยิ่ง เนื่องจากตลาดผลิตภัณฑ์ทางการแพทย์ส่วนใหญ่มีการผลิตตามสัญญาและว่าจ้างหน่วยงานภายนอกให้กับโรงงานขององค์กรอื่นๆ ดังนั้นจึงเป็นความรับผิดชอบขององค์กรที่ทำสัญญาที่จะต้องตรวจสอบให้แน่ใจว่าซัพพลายเชนทั้งหมดเป็นไปตามมาตรฐาน UDI และผลิตฉลากที่ถูกต้อง
ต้นกำเนิดเทคโนโลยีการระบุหมายเลขเฉพาะประจำอุปกรณ์
UDI เป็นตัวระบุอุปกรณ์แบบคงที่ อย่างไรก็ตาม การเปลี่ยนแปลงปริมาณของสินค้าในแพ็คเกจอาจทำให้จำเป็นต้องมีการระบุใหม่ โดยหน่วยงานที่ออกตัวระบุจะกำหนดวิธีแยกแยะรายละเอียดเหล่านี้ ในทำนองเดียวกัน การเปลี่ยนแปลงสภาวะการปลอดเชื้อในบรรจุภัณฑ์ของอุปกรณ์อาจเปลี่ยนแปลงตัวระบุอุปกรณ์ด้วย และการเปลี่ยนตลาดปลายทางของอุปกรณ์ (ประเทศที่จะขายอุปกรณ์) ภาษาของฉลาก หรือเครื่องหมาย CE อาจจำเป็นต้องเปลี่ยนแปลงตัวระบุอุปกรณ์ด้วย
ก่อนที่จะมีกฎ UDI ผู้ผลิตอุปกรณ์ทางการแพทย์อาจติดฉลากผลิตภัณฑ์พร้อมหมายเลขชิ้นส่วนเฉพาะ ผู้จัดจำหน่ายจะเปลี่ยนหมายเลขชิ้นส่วนนั้นก่อนที่ผู้ให้บริการด้านสุขภาพหรือโรงพยาบาลจะเปลี่ยนอีกครั้ง ด้วยความเป็นไปได้ที่ทุกองค์กรจะเปลี่ยนแปลงหมายเลขชิ้นส่วนก่อนถึงมือผู้ป่วย การติดตามผลิตภัณฑ์ จัดการการเรียกคืน ป้องกันการปลอมแปลง หรือสั่งสต็อคใหม่อย่างมีประสิทธิภาพจึงแทบจะเป็นไปไม่ได้เลย
บทความที่เกี่ยวข้อง: การใช้โซลูชันการตรวจสอบย้อนกลับที่แข็งแกร่ง
ในปัจจุบัน ตัวระบุที่เป็นมาตรฐานและถาวรที่เรียกว่า UDI จะถูกติดเข้ากับทุกอุปกรณ์เพื่อให้หน่วยงานทั้งหมดสามารถระบุอุปกรณ์ได้รวดเร็วและแม่นยำยิ่งขึ้น ซึ่งช่วยลดข้อผิดพลาดทางการแพทย์ได้ในที่สุด โดย UDI นี้เป็นรหัสตัวอักษรและตัวเลขที่ประกอบด้วยข้อมูลสำคัญสองส่วน:
- ตัวระบุอุปกรณ์
- ตัวระบุการผลิต
ตัวระบุอุปกรณ์คือป้ายกำกับแบบคงที่ที่กำหนดให้กับอุปกรณ์ที่ระบุ โดยแสดงรายการผู้ติดป้ายกำกับ (โดยทั่วไปคือผู้ผลิตอุปกรณ์) และหมายเลขรุ่นเฉพาะของอุปกรณ์ ในทางตรงกันข้าม ตัวระบุการผลิตประกอบด้วยข้อมูลที่สามารถเปลี่ยนแปลงได้ และข้อมูลส่วนใหญ่ที่สามารถมีได้นั้นเป็นทางเลือก ซึ่งอาจรวมถึงรหัสล็อตและชุดงาน หมายเลขประจำเครื่อง วันหมดอายุ และวันที่ผลิต กล่าวโดยสรุป ข้อมูลเสริมอาจเป็นอะไรก็ได้ที่ผู้ผลิตหรือผู้ติดฉลากเห็นว่าจำเป็นเพื่อสนับสนุนการติดตามอุปกรณ์
ป้าย UDI ทุกป้ายจะต้องนำเสนอข้อมูลนี้ในสองรูปแบบ:
- รูปแบบที่มนุษย์สามารถอ่านได้ (ข้อความธรรมดา)
- แบบฟอร์มที่เครื่องอ่านได้ (อ่านได้ด้วยบาร์โค้ดหรือเครื่องอ่าน RFID)
ไม่ว่าอุปกรณ์จะสามารถตอบสนองการใช้งานทางการแพทย์ได้หลากหลายก็ตาม UDI จะต้องถูกทำเครื่องหมายบนอุปกรณ์โดยตรง ไม่ใช่บนบรรจุภัณฑ์ กฎนี้ยังใช้กับอุปกรณ์ที่สามารถใช้งานได้หลายครั้งด้วย
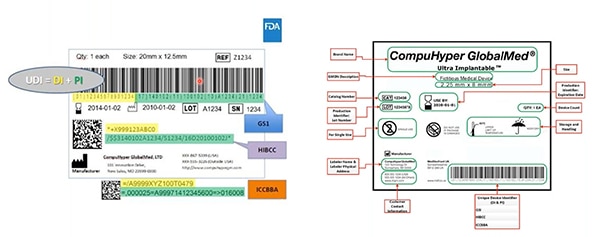 รูปที่ 2: GS1, HIBCC และ ICCBBA — หน่วยงานที่ออก UDI— สร้าง UDI กำหนดสัญลักษณ์ที่อนุญาตของ UDI กำหนดเทคโนโลยีที่สามารถเชื่อมต่อกับ UDI ได้ และระบุคุณภาพที่ต้องการของเครื่องหมาย UDI ไฮไลต์ด้วยสีเหลืองในตัวอย่างนี้คือตัวระบุอุปกรณ์ ที่เน้นด้วยสีเขียวคือตัวระบุการผลิต องค์ประกอบอื่นๆ ได้แก่ ข้อมูลที่มนุษย์อ่านได้และยังมีการเข้ารหัสลงในบาร์โค้ดที่เครื่องอ่านได้ด้วย (แหล่งที่มาภาพ: FDA)
รูปที่ 2: GS1, HIBCC และ ICCBBA — หน่วยงานที่ออก UDI— สร้าง UDI กำหนดสัญลักษณ์ที่อนุญาตของ UDI กำหนดเทคโนโลยีที่สามารถเชื่อมต่อกับ UDI ได้ และระบุคุณภาพที่ต้องการของเครื่องหมาย UDI ไฮไลต์ด้วยสีเหลืองในตัวอย่างนี้คือตัวระบุอุปกรณ์ ที่เน้นด้วยสีเขียวคือตัวระบุการผลิต องค์ประกอบอื่นๆ ได้แก่ ข้อมูลที่มนุษย์อ่านได้และยังมีการเข้ารหัสลงในบาร์โค้ดที่เครื่องอ่านได้ด้วย (แหล่งที่มาภาพ: FDA)
อุปกรณ์ทั้งหมดจะต้องลงทะเบียนในฐานข้อมูล UDI ทั่วโลกเพื่อให้สามารถติดตามได้ในกรณีที่มีการเรียกคืน และเพื่อให้สาธารณะสามารถเข้าถึงข้อมูลเกี่ยวกับอุปกรณ์ที่กำหนดได้ หน่วยงานออกใบรับรองที่ได้รับการรับรองจาก FDA ได้รับอนุญาตให้สร้างตัวระบุเฉพาะสำหรับผู้ผลิตอุปกรณ์เพื่อนำไปติดบนผลิตภัณฑ์ของตน
เอกสารที่เกี่ยวข้อง: ติดตามการตรวจสอบย้อนกลับอยู่เสมอ
เทคโนโลยีและเทคนิคการสแกน UDI
สามารถตรวจสอบฉลาก UDI ได้หลายวิธีตลอดการเดินทางตั้งแต่การผลิตจนถึงการใช้งาน
การตรวจสอบความถูกต้องแบบอินไลน์ดำเนินการโดยเทคโนโลยีที่รวมอยู่ในเครื่องจักรขนาดใหญ่ เพื่อการประมวลผลผลิตภัณฑ์จำนวนมากที่รวดเร็วและแม่นยำในขณะที่ผลิต จากการที่ได้รับการสนับสนุนจากซอฟต์แวร์ขั้นสูง เทคโนโลยีเหล่านี้จึงอยู่ในรูปแบบของเครื่องพิมพ์ฉลากระดับอุตสาหกรรมเป็นครั้งคราว โดยเครื่องพิมพ์เหล่านี้สามารถตรวจสอบความถูกต้องแบบอินไลน์ของตนเองได้ เพื่อยืนยันว่าข้อมูล UDI สามารถอ่านได้ตามมาตรฐานอุตสาหกรรมที่เข้มงวดทันทีเมื่อมีการสร้าง ณ จุดผลิตฉลาก ตัวอย่างเช่น เครื่องตรวจสอบ Omron Automation V275 มีไว้สำหรับใช้กับเครื่องพิมพ์ความร้อน Zebra เพื่อให้เป็นไปตามมาตรฐาน ISO 15426 และหน่วยงานผู้ออก GS1 มาตรฐานการปฏิบัติตามข้อกำหนดของ FDA
ที่เกี่ยวข้อง: โซลูชันการตรวจสอบย้อนกลับของ Omron
นอกจากนั้นการตรวจสอบแบบอินไลน์ใช้รูปแบบของสายพานลำเลียงขนาบข้างด้วยวิชันซิสเต็มวิชันพิเศษในสายการผลิตอัตโนมัติ โดยรวมการอ่านบาร์โค้ดเข้าด้วยกันเพื่อการตรวจสอบการติดฉลาก UDI ที่รวดเร็วและแม่นยำอย่างยิ่งบนผลิตภัณฑ์ที่มีส่วนผสมสูงในสายการผลิตที่มีความเร็วสูง Omron Automation MicroHAWK ข้อเสนอที่เป็นเลิศในด้านนี้ด้วยเซ็นเซอร์ขั้นสูงเสริมด้วยโครงสร้างขนาดเล็กและตัวเลือกการเชื่อมต่อซึ่งรวมถึง Ethernet/IP และ PROFINET
บทความที่เกี่ยวข้อง: หลีกเลี่ยงความรับผิดของการติดฉลากที่ไม่ถูกต้อง
ในทางตรงกันข้าม การตรวจสอบ UDI แบบออฟไลน์เหมาะสมที่สุดสำหรับการสุ่มตัวอย่างฉลากเป็นชุดเพื่อรับประกันคุณภาพ มักใช้สำหรับการทดสอบตัวอย่างเมื่ออุปกรณ์ทางการแพทย์ออกหรือมาถึงสถานพยาบาล การตรวจสอบแบบออฟไลน์สามารถเสริมระบบการตรวจสอบแบบออนไลน์ต้นน้ำในเส้นทางการจัดจำหน่าย
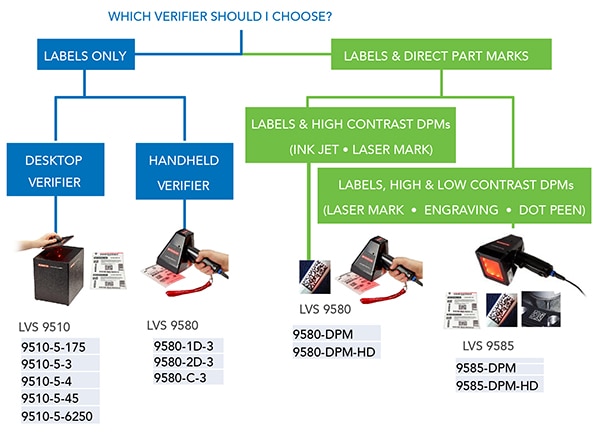 รูปที่ 3: UDI ที่ทำเครื่องหมายโดยตรงบนผลิตภัณฑ์ต้องใช้ตัวตรวจสอบที่แตกต่างจากที่ใช้สำหรับ UDI ที่พิมพ์บนฉลากที่ติดอยู่ (แหล่งที่มาภาพ: Omron Automation)
รูปที่ 3: UDI ที่ทำเครื่องหมายโดยตรงบนผลิตภัณฑ์ต้องใช้ตัวตรวจสอบที่แตกต่างจากที่ใช้สำหรับ UDI ที่พิมพ์บนฉลากที่ติดอยู่ (แหล่งที่มาภาพ: Omron Automation)
ในความเป็นจริงแล้ว การดำเนินการจัดจำหน่ายทางการแพทย์และการดูแลสุขภาพทั้งหมดจะได้รับประโยชน์จากการใช้เครื่องตรวจสอบตามมาตรฐาน ISO ลองพิจารณาผลิตภัณฑ์ตรวจสอบ UDI ออฟไลน์ซีรีส์ LVS 95XX ของ Omron โดยอุปกรณ์เหล่านี้ถูกใช้ใน:
- จุดทำเครื่องหมายด้วยเลเซอร์และเครื่องพิมพ์ฉลากที่มีการสร้างรหัส
- ในกรณีที่มีการใช้รหัสกับผลิตภัณฑ์ซึ่งอาจแยกจากพื้นที่การสร้างรหัสหรือไม่ก็ได้
- ในสถานีควบคุมคุณภาพที่มีการยืนยันเทมเพลต การจัดรูปแบบ และองค์ประกอบโค้ดอื่นๆ
การระบุรูปแบบตัวตรวจสอบ UDI ออฟไลน์
ตัวตรวจสอบ UDI ออฟไลน์ที่เหมาะสมที่สุดสำหรับการใช้งานที่กำหนดนั้นขึ้นอยู่กับพารามิเตอร์หลายตัว
ขนาดบาร์โค้ด: บาร์โค้ดขนาดใหญ่มักจะสแกนได้ง่ายกว่าด้วยตัวระบุที่มีขอบเขตการมองเห็นกว้างซึ่งกำหนดโดยทางยาวโฟกัสของเลนส์และขนาดเซ็นเซอร์ โดยพิจารณาตัวระบุ UDI แบบตั้งโต๊ะ LVS-9510 ของ Omron Automation ผลิตภัณฑ์ซีรีส์นี้สามารถอ่านได้ทั้งฉลากเชิงเส้นและ 2D โดยผลิตภัณฑ์ห้ารุ่นที่แตกต่างกันแต่ละรุ่นมีมุมมองที่แตกต่างกัน ดังนั้นนักออกแบบจึงสามารถเลือกให้เข้ากันได้กับขนาดของบาร์โค้ดที่ต้องได้รับการตรวจสอบ คุณสมบัติการสติชช่วยให้สามารถจัดระดับบาร์โค้ดได้เกินขอบเขตการมองเห็น
นอกจากนี้ LVS-9510 ทั้งหมดสามารถกำหนดสัญลักษณ์และรูรับแสงที่จำเป็นในการประเมินโค้ดและระบุและเน้นจุดที่มีปัญหาได้โดยอัตโนมัติ
 รูปที่ 4: การตรวจสอบบาร์โค้ดที่ตรงตามมาตรฐาน ISO ทำได้ง่ายขึ้นด้วยอุปกรณ์ที่สามารถตรวจสอบรหัสเชิงเส้น (1D) และรหัสสองมิติ (2D) อุปกรณ์ดังกล่าวจะกำหนดสัญลักษณ์และช่องรับแสงที่จำเป็นในการประเมินโค้ด รวมถึงระบุและเน้นปัญหาต่างๆ โดย LVS-9510 ที่แสดงไว้ที่นี่มีคุณสมบัติสติชที่ช่วยให้การจัดระดับบาร์โค้ดมีขนาดใหญ่กว่าขอบเขตการมองเห็น (แหล่งที่มาภาพ: Omron Automation)
รูปที่ 4: การตรวจสอบบาร์โค้ดที่ตรงตามมาตรฐาน ISO ทำได้ง่ายขึ้นด้วยอุปกรณ์ที่สามารถตรวจสอบรหัสเชิงเส้น (1D) และรหัสสองมิติ (2D) อุปกรณ์ดังกล่าวจะกำหนดสัญลักษณ์และช่องรับแสงที่จำเป็นในการประเมินโค้ด รวมถึงระบุและเน้นปัญหาต่างๆ โดย LVS-9510 ที่แสดงไว้ที่นี่มีคุณสมบัติสติชที่ช่วยให้การจัดระดับบาร์โค้ดมีขนาดใหญ่กว่าขอบเขตการมองเห็น (แหล่งที่มาภาพ: Omron Automation)
ประเภทบาร์โค้ด: เครื่องสแกนจะต้องอ่านรูปแบบบาร์โค้ดตามที่กำหนดโดยหน่วยงานที่ออกซึ่งเรียกว่า HIBCC, ICCBBA หรือ (โดยทั่วไปในปี 2023) GS1 โดย GS1 กำหนดขนาด รูปแบบ และความละเอียดของ UPC บาร์โค้ดเชิงเส้น และบาร์โค้ดเมทริกซ์ข้อมูล 2D
ตำแหน่งเครื่องหมาย UDI: พิจารณาการมาร์กชิ้นส่วนโดยตรง (DPM) ของอุปกรณ์ทางการแพทย์ เครื่องหมายเหล่านี้อาจมีขนาดเล็กมาก โดยเฉพาะอย่างยิ่งเมื่ออยู่บนเครื่องมือผ่าตัดและอุปกรณ์ทางการแพทย์ เพื่ออ่านและตรวจสอบ DPM UDI ดังกล่าว เครื่องตรวจสอบแบบพกพาที่มีความหนาแน่นสูงพิเศษ LVS-9580 และ LVS-9585 ของ Omron มีเลนส์พิเศษที่สามารถจัดระดับ DPM มากมาย รวมถึงเลนส์ที่มีขนาดเซลล์ต่ำถึง 0.002 นิ้ว โดยเลนส์เกรดอุตสาหกรรมภายใน LVS-9580 และ LVS-9585 ช่วยให้มั่นใจถึงความแม่นยำในการอ่านที่สม่ำเสมอ สิ่งที่ซับซ้อนที่สุดคือเทคโนโลยีแสงสว่างที่ควบคุมและสอบเทียบได้สูงภายในเครื่องสแกน นอกจากขอบเขตการมองเห็นที่หลากหลายแล้ว การจัดแสงยังช่วยเพิ่มประสิทธิภาพให้กับภาพ UDI ที่ถ่ายได้ทันที ซึ่งสิ่งนี้มีความสำคัญอย่างยิ่งเนื่องจากมาตรฐานโค้ดไม่อนุญาตให้มีการแก้ไขหรือปรับแต่งรูปภาพในภายหลัง
ข้อมูลเพิ่มเติมเกี่ยวกับซอฟต์แวร์สแกนเนอร์ UDI
เพื่อประสิทธิภาพสูงสุด ซอฟต์แวร์ UDI ที่รองรับฮาร์ดแวร์ตัวตรวจสอบจะต้องนำเสนอข้อมูลการวินิจฉัยในรูปแบบที่ใช้งานง่าย โดยซอฟต์แวร์นี้จะต้องให้คะแนนรหัส UDI ตามพารามิเตอร์ที่กำหนดโดย ISO (ที่สำคัญที่สุดคือเพื่อยืนยันความสามารถในการอ่าน) และควรติดตามปัญหาจากการสแกน UDI หลายชุดด้วยเช่นกัน
Omron มีซอฟต์แวร์ที่จำเป็นทั้งหมดพร้อมกับฮาร์ดแวร์สแกน UDI ทุกตัว ซอฟต์แวร์ได้รับการอัปเดตเป็นประจำเพื่อให้ทันกับกฎระเบียบที่พัฒนาอย่างรวดเร็วและกฎหมายอุตสาหกรรมใหม่
หน้าที่หลักของซอฟต์แวร์สแกนเนอร์ Omron คือการจัดการโครงสร้างของโค้ด กล่าวโดยสรุป บาร์โค้ดหรือโค้ด 2D ทุกอันจะต้องดึงข้อมูลที่เกี่ยวข้องทั้งหมดอย่างถูกต้อง รวมถึงประเภทผลิตภัณฑ์ หมายเลขล็อต ปริมาณตามที่เกี่ยวข้อง วันหมดอายุ ข้อมูลการจัดส่ง ฯลฯ สตริงข้อมูลที่ได้จะต้องจัดรูปแบบในลักษณะเฉพาะเพื่อให้ทันกับข้อกำหนดที่เปลี่ยนแปลงไป วิธีการและปลายทางผลิตภัณฑ์ทางการแพทย์
ซอฟต์แวร์ที่ได้รับการอัปเดตเป็นประจำจากผู้ผลิตสแกนเนอร์ทำให้ผู้ใช้ปลายทางได้รับข้อมูลล่าสุดอยู่เสมอ แม้ว่าจะมีการเปิดตัวมาตรฐานใหม่ก็ตาม
สรุป
ครั้งหนึ่งกองทัพสหรัฐฯ มีเป้าหมายที่จะใช้ระบบติดตามผลิตภัณฑ์ UID อย่างเต็มรูปแบบ เช่น ระบบ UDI ของอุตสาหกรรมการแพทย์ จุดประสงค์คือเพื่อลดปริมาณขยะจำนวนมหาศาลที่เกี่ยวข้องกับสิ่งของสูญหาย ซ้ำซ้อน และนับไม่ถ้วนในสถานที่ปฏิบัติงานทางทหาร รวมถึงทุกอย่างตั้งแต่อาวุธของ Raytheon ที่เสร็จสมบูรณ์ไปจนถึงแผงควบคุมที่จัดหาโดยชุดเล็กๆ สำหรับการใช้งานเฉพาะทางบางอย่าง ปัจจุบัน UID มีระดับการใช้งานที่หลากหลาย
สิ่งเดียวกันนี้จะไม่เป็นชะตากรรมของข้อบังคับ UDI
สิ่งที่ขับเคลื่อนการนำ UDI มาใช้นั้นตรงไปตรงมา:ฉลากคือสินค้า ท้ายที่สุดแล้ว การติดฉลากที่ไม่ถูกต้องอาจทำให้เกิดเหตุการณ์ต่อเนื่องจนทำให้เจ้าหน้าที่ทางการแพทย์ต้องเสียเวลาและส่งผลให้อุปกรณ์ทางการแพทย์ถูกทิ้ง ดังนั้น UDI จะต้องปรากฏบนบรรจุภัณฑ์ทุกระดับ เช่น ในระดับหน่วย บรรจุภัณฑ์ มัด กล่อง และพาเลท โดย UDI บนอุปกรณ์ทางการแพทย์ปลอดเชื้อภายในซีลฆ่าเชื้อมีความสำคัญเป็นพิเศษ เนื่องจากการฉีกซีลเพื่อยืนยันไม่สามารถยอมรับอุปกรณ์นั้นได้
เนื่องจาก FDA กำหนดให้ต้องปฏิบัติตามคำสั่ง UDI อย่างเต็มรูปแบบตั้งแต่วันที่ 24 กันยายน 2023 เทคโนโลยีการสแกนขั้นสูงสำหรับการตรวจสอบผลิตภัณฑ์ทางการแพทย์จึงมีความสำคัญอย่างยิ่งต่อผู้ผลิตระบบอัตโนมัติ รวมถึงผู้ผลิตเครื่องจักรและผู้ใช้ปลายทางที่พวกเขาให้บริการ
เครื่องสแกนดังกล่าวสามารถตอบสนองข้อกำหนด FDA UDI ที่เฉพาะเจาะจงอย่างยิ่ง เพื่อยืนยันฉลากบนอุปกรณ์ห้องปฏิบัติการ การแพทย์ และการวินิจฉัยทางคลินิกที่หลากหลาย เครื่องตรวจสอบบาร์โค้ดแบบออฟไลน์ เพิ่มความสามารถในการตรวจสอบย้อนกลับ การมองเห็นของเครื่องจักรแบบอินไลน์ และเครื่องอ่าน DPM ขั้นสูง

Disclaimer: The opinions, beliefs, and viewpoints expressed by the various authors and/or forum participants on this website do not necessarily reflect the opinions, beliefs, and viewpoints of DigiKey or official policies of DigiKey.






